电位滴定法是通过电位的变化来确定滴定终点的方法,特别适用于化学反应的平衡常数较小、滴定突跃不明显或试液有色、呈现浑浊的情况。通常确定终点的有以下4种方法。
电位滴定的仪器装置如图1 所示。试液中插入指示电极和参比电极构成工作电池,滴定过程不断测量工作电池电动势的变化,达化学计量点时,由于浓度的突变,引起指示电极电位突变,而使工作电池电动势发生突变,从而指示滴定终点的到达。本法可用于酸碱滴定、氧化还原滴定、沉淀滴定和配合物滴定。根据待测离子性质的不同,选用的指示电极和参比电极如表1 所示。
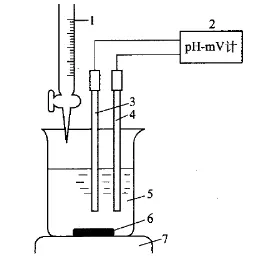
图1 电位滴定仪器装置1-滴定管;2-pH-mV计;3-指示电极;4-参比电极;5-试液;6-搅拌子;7-电磁搅拌器
表1 电位滴定常用的电极

电位滴定法中,确定滴定终点的方法有以下几种。现以用0.1mol/L AgNO3标准溶液滴定氯离子的数据为例,予以说明。
1.绘φ-V曲线法以加入滴定剂的体积(V)作为横坐标,以测得工作电池的电动势(φ)作为纵坐标,绘制φ-V滴定曲线,曲线上的转折点即为滴定终点,如图2 (a)所示。
2.绘
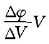
曲线法又称一级微商法,
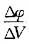
为φ的变化值与相对应加入滴定体积V的增量之比,如加入滴定剂在24.10mL和24.20mL,则:

表2 以0.1mol/L AgNO3溶液滴定NaCl溶液

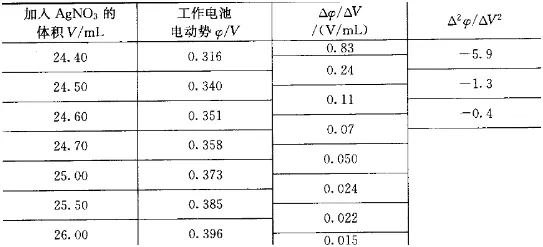
用表2 中
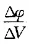
值对V作图,如图2 (b)所示,获一呈现尖峰极大的曲线,尖峰极大值所对应的V值,即为滴定终点,约为24.30~24.40mL。
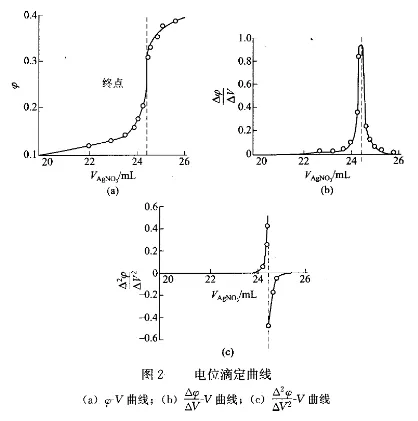
3.绘
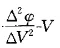
曲线法通常一级微商曲线的极大值为终点,则其二级微商必定等于零,
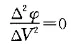
,此点也为终点,见图2 (c)。
计算如下:在24.30mL处
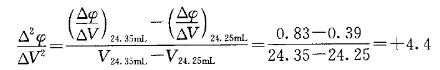
在24.40mL处
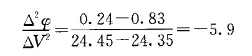
用内插法可计算出化学计量点的体积(Ve)和电动势(φe)。
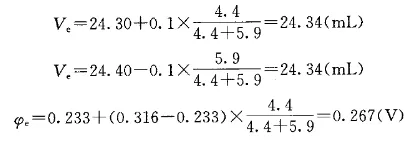
4.电位滴定法测定水泥生料中的钙含量本测定中使用钙离子选择性电极作为指示电极,饱和甘汞电极作为参比电极构成工作电池。当Ca2+含量在10-5~10-1 mol/L范围内,钙离子选择性电极响应呈线性。测定适用的pH值范围为5~10,可采用NH4OH-NH4CI或硼砂-NaOH缓冲液来调节试液的pH值。测定时Fe3+、Al3+、Zn2+、Pb2+会干扰Ca2+的测定,可加入少量三乙醇胺来掩蔽干扰离子。
水泥生料试样先用少量水润湿,再用3mol/L盐酸溶液溶解,煮沸、过滤并稀释至一定体积。取一定量试液加入少量三乙醇胺和硼砂缓冲溶液,用标准EDTA溶液滴定,使用ZD-2型自动电位滴定仪,记录滴定过程工作电池电动势的变化,绘制
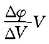
曲线可确定滴定终点。重复测定五次,取所用滴定剂体积的平均值计算水泥生料中的钙含量。